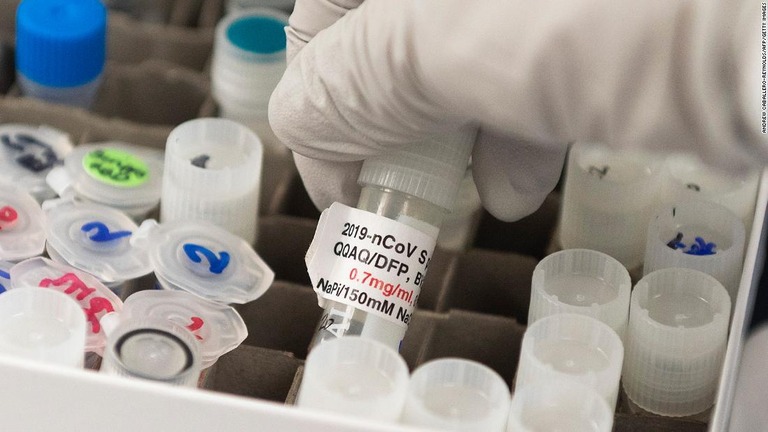
米FDA諮問委、ノババックス製ワクチンの緊急使用許可を検討へ
(CNN) 米食品医薬品局(FDA)の諮問委員会は7日、米ノババックス製の新型コロナウイルスワクチンについて、緊急使用許可(EUA)を出すかどうかを検討する。
FDAは3日に公開した文書の中で、ノババックス製ワクチンは軽症から中等症、重症の新型コロナ感染症に対し、接種完了後2カ月半にわたって90.4%の効果が認められたと報告した。一方、65歳以上の成人では、効果が78.6%に落ちるとみられる。
ただし、これはオミクロン株の流行より前に得られた数字で、オミクロン株に対する効果やその持続期間は明らかでない。ノババックスは昨年12月、オミクロン株などの変異株にも幅広い効果を示すと主張していた。
同社のワクチンはまず3週間の間隔で2回、さらに6カ月後に3回目を接種する。
副反応はほとんどが軽度から中等度で、2~3日のうちに収まっている。ただFDAは文書の中で、心筋炎や心膜炎がまれながら少数、ワクチンとの因果関係が懸念されるタイミングで報告されていると指摘した。
それによると、ノババックス製ワクチンの接種後に発症したのは6人で、このうち5人は16~67歳の男性。6人中5人が病院に収容されたが、その後回復している。
心筋炎、心膜炎のリスク増大は、米国内で現在使われている米ファイザー製、モデルナ製のワクチンでも指摘されていた。