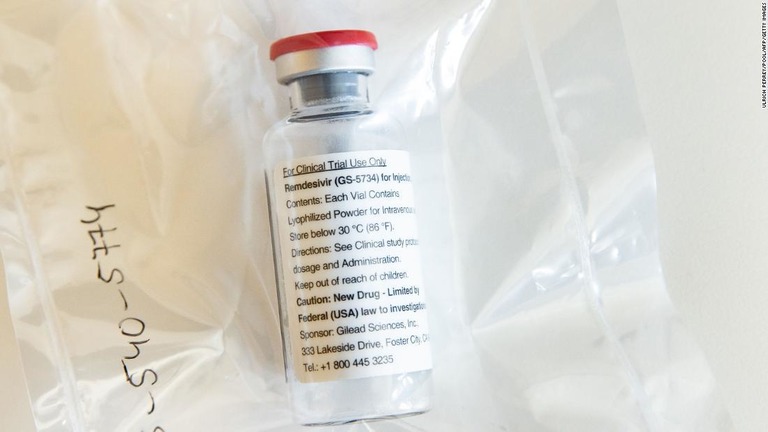
米FDA、レムデシビルの緊急使用を許可 入院中の重症患者対象
(CNN) 米食品医薬品局(FDA)は1日、治験薬「レムデシビル」について、新型コロナウイルス感染症で入院中の重症患者に対する緊急使用を許可した。
FDAのスティーブン・ハーン長官によると、新型コロナの治療薬として米国で許可されたのはレムデシビルが初めて。
ハーン氏は今回の許可を「臨床上の重要な前進」と評価。レムデシビルの投与で「新型コロナ患者の回復期間に統計的に有意な短縮がみられた」と説明した。
FDAは緊急使用を許可した理由について、患者への恩恵がリスクを上回るためとしている。緊急使用許可はFDAによる全面的な承認に比べ、規制上のハードルが低い。
FDAの研究責任者、デニス・ヒントン氏は許可を発表した書簡の中で、「レムデシビルの緊急使用以外には、適切かつ承認済みで利用可能な新型コロナ感染症の治療法は存在しない」と指摘した。
FDAはレムデシビルの使用許可を、血中酸素濃度が低下していたり、酸素治療や人工呼吸器などによる集中的な呼吸補助が必要だったりする重症患者に限定する方針を示した。
レムデシビルの副作用としては、肝酵素値の上昇や血圧低下、吐き気、おう吐、発汗、悪寒などがあり得るという。肝酵素値の上昇は、肝細胞の炎症や損傷の兆候となる可能性がある。
トランプ米大統領は1日、ホワイトハウスの執務室でレムデシビルに触れ、「状況は非常に明るい」と述べた。
レムデシビルを開発した米製薬大手ギリアド・サイエンシズは既に、新型コロナ患者向けに少なくとも14万人分の在庫を寄付しており、さらに10月までに少なくとも50万人分、12月までに100万人分、来年には数百万人分を製造する目標を掲げている。