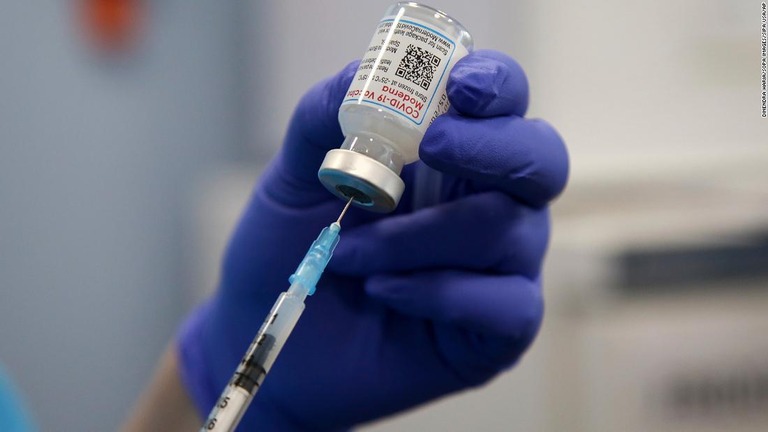
米モデルナ、BA.5対応ワクチンの緊急使用許可を申請 ファイザーに続き
(CNN) 米モデルナは23日、新型コロナウイルスのオミクロン株の新系統「BA.4」「BA.5」に対応するワクチンを、18歳以上に対する追加接種として使うための緊急使用許可(EUA)を、米食品医薬品局(FDA)に申請したと発表した。
現行のワクチンとBA.4、BA.5対応の成分を混ぜた「2価ワクチン」で、1回分が50マイクログラム。
現在、臨床試験(治験)が進められているという。同社がFDAに提出したデータにはマウスを使った実験や、オミクロン株の「BA.1」系統に対応する追加接種用ワクチンの治験結果が含まれている。
モデルナのバンセル最高経営責任者(CEO)は、新たな2価ワクチンの効果について、現行の追加接種用ワクチンよりさらに強く、幅広く、長続きする可能性があると述べた。
米ファイザーと独ビオンテックも22日、BA.5対応の2価ワクチンを、12歳以上への追加接種に使うためのEUAを申請したと発表していた。
ホワイトハウスのジャー新型コロナ対策調整官は最近、改良型の追加接種用ワクチンが来月初めから半ばには接種可能になるとの見通しを示したが、そのタイミングはFDAがいつ許可を出すかにかかっている。
FDAは、過去の変異株に対応したワクチンなども含めたデータから総合的に判断を下すとしている。その前に専門家による諮問会議を開いた場合は、接種開始の時期が遅れる可能性もある。